Résumé.
Plus une masse d'air contient de l'eau et plus elle contient une quantité de chaleur importante.
Et donc plus cette masse d'air humide possède une inertie thermique élevée.
Et donc plus cette masse d'air humide possède une inertie thermique élevée.
Chaleurs latente et sensible de l'eau.
Il est déjà clair à ce stade-ci de l'étude que la masse de matière est capitale et gouverne un climat à la base car plus il y a de la masse, plus il y a de chaleur. On sait aussi que la masse d'un m3 de roche est généralement plus grande que la masse d'un m3 d'eau qui elle-même est plus élevée que la masse d'un m3 d'atmosphère.
En comparant (voir ci-dessous) les chaleurs d'un sauna et d'un hammam, qui en terme de quantité peuvent être identiques alors que leurs températures sont très différentes, on comprend déjà que l'eau joue un rôle très important dans l'accumulation de chaleur.
Le véritable enjeu de cette étude est la quantité de chaleur, et la plupart du temps, celle-ci peut être traduite par la masse, mais dans le cas de la molécule d'eau, les choses deviennent plus complexes et il faut alors s'exprimer avec cette notion de quantité de chaleur.
Une atmosphère humide contient beaucoup plus de chaleur qu'une atmosphère sèche : il s'agit non seulement de la chaleur sensible mais aussi de la chaleur latente qui est contenue dans la molécule d'eau.
Si la chaleur sensible est la chaleur que l'on sent et dont on mesure la température, la chaleur latente contenue dans la molécule d'eau est la chaleur qui est responsable de la formation des ouragans, c'est une chaleur de changement d'état (solide <--> liquide <--> gazeux). Or l'eau est la seule molécule de l'atmosphère pouvant changer d'état aux températures et pressions régnant sur Terre.
Cette caractéristique contenue au sein de la molécule d'eau suffit à l'ériger en tant que molécule exceptionnelle. Aucune autre molécule présente dans l'atmosphère ne peut prétendre de près ou de loin à avoir la faculté de créer quelque chose d'aussi exceptionnel et concret qu'un ouragan.
En conclusion, un air humide contient plus de chaleur qu'un air sec car : la quantité d'eau est plus importante et l'eau a la capacité d'échanger la chaleur latente.
Comparaison sauna / hammam :
Si vous faites l'expérience de divers saunas et hammams, vous constatez par exemple que dans un sauna à 85°C et 15% d'humidité, vous avez la même sensation de chaleur que dans un hammam à 50°C et 100% d'humidité. Ceci n'est pas qu'une sensation dépendant de votre état interne, c'est d'abord une quantité de chaleur qui est à peu près égale dans ces deux cas. Cette quantité se répartit dans les molécules d'air et dans les molécules d'eau. Il y a beaucoup plus de chaleur dans une molécule d'air ou d'eau d'un sauna (85°C) que dans une molécule d'air ou d'eau d'un hammam (50°C), mais puisqu'il y a beaucoup plus de molécules d'eau dans un hammam (100%) que dans un sauna (15%), la quantité de chaleur de l'ensemble des molécules d'eau est plus grande dans le hammam, ce qui donne une quantité de chaleur totale (air + eau) équivalente.
Ceci doit être affiné par le fait que dans un hammam, l'humidité de l'air se colle à la peau et permet donc des échanges de chaleur plus facilement. Il n'en reste pas moins qu'en faisant varier les paramètres température et humidité dans deux cas de figure différents, on peut trouver une quantité de chaleur égale.
Si on verse de l'eau sur les pierres d'un sauna, vous avez plus chaud alors que la température reste identique car l'air contient alors plus d'eau chauffée : la quantité d'eau en suspension dans l'air est plus importante et elle transmet alors plus massivement sa chaleur à votre corps (par convection et peut être déjà par conduction); et deuxièmement, cette plus grande transmission de chaleur se fait plus facilement car l'humidité plus importante se colle plus aisément à votre peau et permet ces échanges de chaleur par conduction directe (goutte d'eau --> eau corporelle).
Si on continue à verser de l'eau sur les pierres, les molécules d'eau gazeuses ainsi formées vont remplir de plus en plus l'air du sauna, et à partir d'un certain moment ces molécules vont commencer à s’agréger entre elles, repassant progressivement de l'état gazeux (molécules libres) à l'état liquide (molécules liées).
Si le processus se poursuit, l'agrégation de molécules d'eau sera telle que l'on pourra les voir à l'oeil nu sous forme de fines gouttelettes. (Ce sera alors un sauna devenu hammam, intenable et dangereux).
Ce processus de condensation libère une certaine quantité de chaleur latente qui vient s’ajouter à la quantité de chaleur de base déjà présente dans la masse totale des molécules d'eau et d'air chauffées.
Ceci doit être affiné par le fait que dans un hammam, l'humidité de l'air se colle à la peau et permet donc des échanges de chaleur plus facilement. Il n'en reste pas moins qu'en faisant varier les paramètres température et humidité dans deux cas de figure différents, on peut trouver une quantité de chaleur égale.
Si on verse de l'eau sur les pierres d'un sauna, vous avez plus chaud alors que la température reste identique car l'air contient alors plus d'eau chauffée : la quantité d'eau en suspension dans l'air est plus importante et elle transmet alors plus massivement sa chaleur à votre corps (par convection et peut être déjà par conduction); et deuxièmement, cette plus grande transmission de chaleur se fait plus facilement car l'humidité plus importante se colle plus aisément à votre peau et permet ces échanges de chaleur par conduction directe (goutte d'eau --> eau corporelle).
Si on continue à verser de l'eau sur les pierres, les molécules d'eau gazeuses ainsi formées vont remplir de plus en plus l'air du sauna, et à partir d'un certain moment ces molécules vont commencer à s’agréger entre elles, repassant progressivement de l'état gazeux (molécules libres) à l'état liquide (molécules liées).
Si le processus se poursuit, l'agrégation de molécules d'eau sera telle que l'on pourra les voir à l'oeil nu sous forme de fines gouttelettes. (Ce sera alors un sauna devenu hammam, intenable et dangereux).
Ce processus de condensation libère une certaine quantité de chaleur latente qui vient s’ajouter à la quantité de chaleur de base déjà présente dans la masse totale des molécules d'eau et d'air chauffées.
Complément : effets relatifs de la température et de l'humidité sur la masse de l'air.
Étant donné que la masse moléculaire de l'eau (H2O : 2.1 + 16 = 18) est plus faible que la masse des autres molécules atmosphériques (azote N2 : 2.14 = 28) (oxygène O2 : 2.16 = 32) (argon Ar : 40), et que suivant la loi des gaz parfaits qui veut que le nombre total de molécules dans un certain volume soit toujours identique, si une parcelle d'air devient plus humide, c'est-à-dire si des molécules d'azote et d'oxygène essentiellement sont remplacées par des molécules d'eau, cette parcelle d'air sera donc plus légère. Dans toutes les considérations de masse dont il est question dans cette étude, le passage de l'air sec à l'air humide (ainsi que le passage de l'air chaud à l'air froid) est, contre intuitivement, le seul point où l'on "perd" un peu de masse, et même très peu comme on peut s'en apercevoir dans l'exemple ci-dessous. Cette légère "perte" ne vient donc évidemment pas remettre en question l'effet de masse lié à l'ensemble de la colonne d'air atmosphérique. De plus, la chaleur latente de l'eau fait plus que compenser la diminution de poids.
Si l'air sec est plus lourd, l'air froid est plus lourd également. Un air froid et sec sera donc le plus lourd, à quelques grammes près, mais sera aussi celui qui comporte le moins de chaleur.
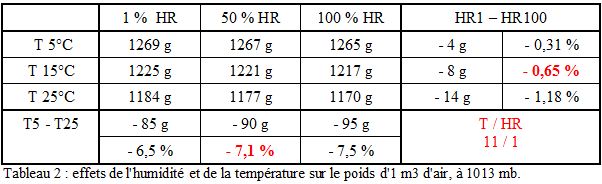
Le tableau 2 indique le poids d'un m3 d'air, en grammes, en fonction de l'humidité relative et de la température, à la pression atmosphérique de 1013 mb :
Si l'air sec est plus lourd, l'air froid est plus lourd également. Un air froid et sec sera donc le plus lourd, à quelques grammes près, mais sera aussi celui qui comporte le moins de chaleur.
Le tableau 2 indique le poids d'un m3 d'air, en grammes, en fonction de l'humidité relative et de la température, à la pression atmosphérique de 1013 mb :
A 5°C, l'air sec (1% HR) pèse 1269 g, et l'air saturé (100% HR) pèse 1265 g, c'est-à-dire 4 g de moins, soit 0.31 % plus léger.
A 15°C, l'air sec pèse 1225 g, et l'air saturé 1217 g c'est-à-dire 0.65 % plus léger.
A 25°C, l'air sec pèse 1184 g, et l'air saturé pèse 1170 g c'est-à-dire 1.18 % plus léger.
Quand on passe de 5°C à 25°C, l'air sec pèse 85 g de moins (-6.7 %), et l'air saturé pèse 95 g de moins (-7.5 %).
Ce qui veut dire qu'en passant de 5°C à 25°C, un m3 d'air, s'allège de +/- 7%, qu'il soit sec ou humide, alors qu'à 15°C, le passage d'un air totalement sec à un air saturé ne s'allège que de 0.65%. Ainsi l'effet de la température sur le poids de l'air est ici 11 fois plus important que l'effet de l'humidité. Si l'on prend des températures de -10°C ou de 40°C, la différence entre les deux effets reste de l'ordre d'un facteur 10. http://www.thermexcel.com/french/tables/massair.htm
Effets relatifs de la température et de l'humidité sur la masse de l'air : cas de figure rencontré par un deltaplane en Suisse à une altitude de 2100m (0.8 bar) où l'air ambiant est à 10°C avec une température de point de rosée (qui est une mesure de l'humidité) de 3°C, et où l'air d'une cellule convective est à 10.5°C avec une température de point de rosée de 4°C. En appliquant la loi des gaz réels (et non pas la loi scolaire des gaz parfaits), un m3 de cet air ambiant (T=10°C et Td=3°C) pèse environ 1 kg; si la température monte à 10.5°C, le m3 d'air sera 1.73 g plus léger, et si l'humidité passe de Td=3°C à Td=4°C, le m3 d'air sera seulement 0.18 g plus léger, et donc au total l'air convectif est 1.91 g plus léger que l'air ambiant. Ce qui veut dire que le rôle de l'humidité est ici 10 fois moins important que le rôle de la température pour expliquer la variation de la masse de l'air. http://www.soaringmeteo.ch/SG_flottabTh.pdf
A 15°C, l'air sec pèse 1225 g, et l'air saturé 1217 g c'est-à-dire 0.65 % plus léger.
A 25°C, l'air sec pèse 1184 g, et l'air saturé pèse 1170 g c'est-à-dire 1.18 % plus léger.
Quand on passe de 5°C à 25°C, l'air sec pèse 85 g de moins (-6.7 %), et l'air saturé pèse 95 g de moins (-7.5 %).
Ce qui veut dire qu'en passant de 5°C à 25°C, un m3 d'air, s'allège de +/- 7%, qu'il soit sec ou humide, alors qu'à 15°C, le passage d'un air totalement sec à un air saturé ne s'allège que de 0.65%. Ainsi l'effet de la température sur le poids de l'air est ici 11 fois plus important que l'effet de l'humidité. Si l'on prend des températures de -10°C ou de 40°C, la différence entre les deux effets reste de l'ordre d'un facteur 10. http://www.thermexcel.com/french/tables/massair.htm
Effets relatifs de la température et de l'humidité sur la masse de l'air : cas de figure rencontré par un deltaplane en Suisse à une altitude de 2100m (0.8 bar) où l'air ambiant est à 10°C avec une température de point de rosée (qui est une mesure de l'humidité) de 3°C, et où l'air d'une cellule convective est à 10.5°C avec une température de point de rosée de 4°C. En appliquant la loi des gaz réels (et non pas la loi scolaire des gaz parfaits), un m3 de cet air ambiant (T=10°C et Td=3°C) pèse environ 1 kg; si la température monte à 10.5°C, le m3 d'air sera 1.73 g plus léger, et si l'humidité passe de Td=3°C à Td=4°C, le m3 d'air sera seulement 0.18 g plus léger, et donc au total l'air convectif est 1.91 g plus léger que l'air ambiant. Ce qui veut dire que le rôle de l'humidité est ici 10 fois moins important que le rôle de la température pour expliquer la variation de la masse de l'air. http://www.soaringmeteo.ch/SG_flottabTh.pdf
Récapitulatif et mise en perspective des effets.
1. Plus l'atmosphère est massive, plus grande est sa quantité de chaleur (et son inertie thermique) : c'est le principe de base.
2. Une atmosphère riche en eau accroît encore sa quantité de chaleur : cela renforce le principe de base.
3. Plus la température augmente, plus l'air devient léger. Il y a donc un peu moins de masse (contre-effet) mais celle-ci est plus chaude.
4. Plus l'humidité augmente, plus l'air devient léger. Le contre-effet est ici dix fois plus faible que le précédent.
2. Une atmosphère riche en eau accroît encore sa quantité de chaleur : cela renforce le principe de base.
3. Plus la température augmente, plus l'air devient léger. Il y a donc un peu moins de masse (contre-effet) mais celle-ci est plus chaude.
4. Plus l'humidité augmente, plus l'air devient léger. Le contre-effet est ici dix fois plus faible que le précédent.
Quelques sources.
http://www.ouragans.com/faq/sectionC.asp
http://jflemen.iutlan.univ-rennes1.fr/Cmther/calorim.htm
http://www.saunas.eu.com/
http://fr.wikiversity.org/wiki/Changements_d'%C3%A9tats/Vaporisation_et_condensation
Diagramme des phases de l'eau http://science-for-everyone.over-blog.com/categorie-11179567.html
Diagramme des phases de l'azote http://pravarini.free.fr/gaz-Azote.htm
Diagramme des phases de l'oxygène http://pravarini.free.fr/gaz-Oxygene.htm
Diagramme des phases de l'argon http://pravarini.free.fr/gaz-Argon.htm
Diagramme des phases du CO2 http://pravarini.free.fr/CO2.htm
Diagramme des phases du méthane http://pravarini.free.fr/gaz-methane.htm
http://jflemen.iutlan.univ-rennes1.fr/Cmther/calorim.htm
http://www.saunas.eu.com/
http://fr.wikiversity.org/wiki/Changements_d'%C3%A9tats/Vaporisation_et_condensation
Diagramme des phases de l'eau http://science-for-everyone.over-blog.com/categorie-11179567.html
Diagramme des phases de l'azote http://pravarini.free.fr/gaz-Azote.htm
Diagramme des phases de l'oxygène http://pravarini.free.fr/gaz-Oxygene.htm
Diagramme des phases de l'argon http://pravarini.free.fr/gaz-Argon.htm
Diagramme des phases du CO2 http://pravarini.free.fr/CO2.htm
Diagramme des phases du méthane http://pravarini.free.fr/gaz-methane.htm